雙光子激發熒光的優勢就是相比共聚焦使用更長的波長,所以對于組織而言有著更小的傷害,同時,穿透力更深!共聚焦的成像深度普遍在100μm,而雙光子可以達到250μm-500μm,有些甚至能夠達到1mm。另外,同時吸收雙光子僅僅在一個焦點處,所以不會損傷焦平面以外的組織,并且成像更清晰!
更短的脈沖會產生更亮的信號
多光子和高次諧波等非線性依賴于脈沖激光峰值功率。峰值功率的提高,增加了同時發生多光子吸收的概率。例如雙光子熒光與三光子熒光信號分別與入射光強度的平方和三次方成比例。對于激光器峰值功率的增加,相應的激發熒光信號隨之增加。低于50fs的脈沖寬度能夠明顯提高多光子效率和高次諧波產生效率,進而明顯提高成像質量(亮度)。如下圖所示,展示了雙光子(SHG)和三光子(THG)信號強度與脈沖持續時間[1,2](SHG強度-1/τ)之間的關系。
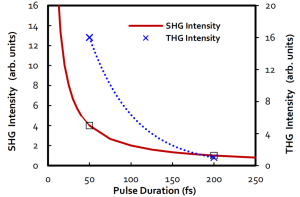
值得一提的是,如果顯微鏡光學器件中的色散沒有得到適當補償,脈沖將被拉伸,并且將在樣品處測量較低的峰值功率。在這種情況下,脈沖持續時間和高次諧波產生效率之間的關系無法通過實驗精確驗證。為了產生足夠的非線性SHG和THG信號,以在對樣本溫和的平均功率水平下實現所需的信噪比,50 fs以下的脈沖和色散預補償的使用是必不可少的。
50fs光纖飛秒激光器——VALO系列
雙光子吸收和頻產生非線性過程,這要求及其強的電場強度,而電場取決于聚焦光斑的大小和激光器脈寬。聚焦光斑越小、脈寬越窄、雙光子吸收效率越高!
基于光纖激光器——VALO,其具有靈活性、易用性和低維護成本。是現代雙光子成像領域得力光源!緊湊型VALO Aalto和VALO Tidal激光器以30MHz的重復頻率提供<50fs的脈沖,單脈沖能量分別是6.6nJ與66nJ,平均功率分別為200mW與2000mW。光束質量無對準的高質量光束(Aalto的典型M2<1.1,Tidal的典型M2<1.2)并且集成了色散預補償模塊。

VALO飛秒激光器采用被動冷卻方式、不需要水冷與風冷散熱。并且前面提及,超短脈沖和更好的光束質量,可以擁有更高的光子轉換效率、并且較低的平均功率對于觀察活體細胞而言,對細胞或組織的損傷更低。
VALO系列飛秒光纖激光器
<50 fs 脈沖持續時間
高達 2 W 的輸出功率
極低的噪音
集成預補償色散模塊
應用實例1
長時間觀察活體細胞過程中,光損傷是限制因素之一。在實驗過程中高平均功率的持續照射對細胞本身產生很大影響。不過,對光毒性敏感的活細胞來說,低平均功率、小于50fs的脈沖寬度、極高的峰值功率,既減少了對細胞的損傷、又大大延長了成像時間。
例如下表統計所示:VALO 50fs與傳統200fs進行比較,同峰值功率只需要輸出1/4的激光功率,換句話來講,成像相同質量情況下,成像效率是傳統200fs激光光源的4倍!同時,相比傳統200fs而言,還能擁有更長的成像時間,為了降低光毒性的影響,更低的重復頻率光源是首選。總的來說,VALO激光器具備這樣的優勢條件。
| 脈沖寬度 | 峰值功率(30MHz) | 平均功率 |
| 200fs | 16KW | 100mW |
| 50fs | 16KW | 25mW |
VALO激光器與傳統激光器參數對比
下圖顯示了使用VALO系列<50fs脈沖激光器在沒有組織損傷的情況下進行髓鞘形態的多光子成像和長時間延時采集(超過一小時)。觀察到脫軸和脫軸髓鞘膜可以研究鈉離子通道在多發性硬化(MS)疾病中的作用。
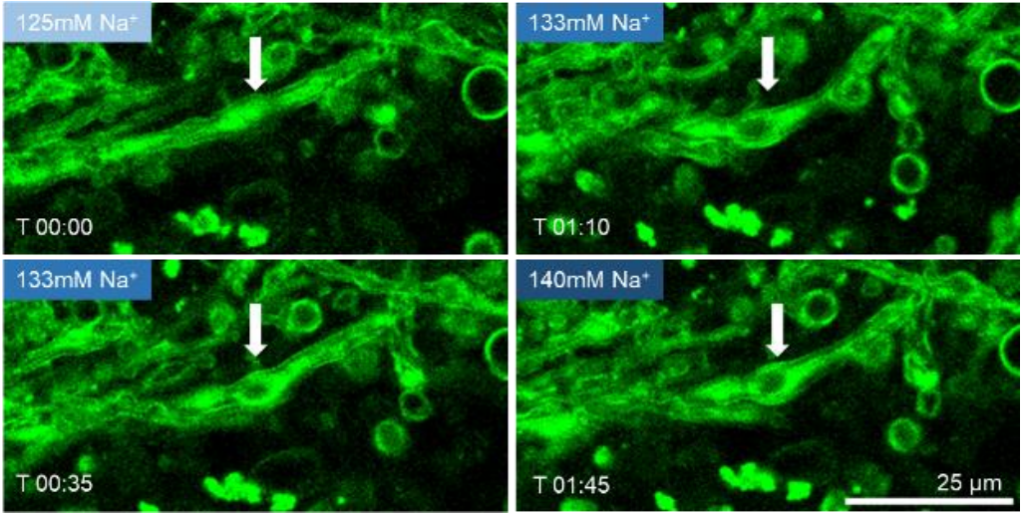
隨著鈉離子濃度持續提高,進而誘導髓鞘腫脹 得到的延時成像
應用實例2
如下圖所示,顯示了來自校準網格的三次諧波信號,樣品的平均功率為4.7mW,具有VALO系列飛秒激光器的全帶寬,產生約40fs脈沖。在圖b)中,激光器的光譜帶寬被限制在1064nm附近的10nm FWHM,產生約160 fs的脈沖。圖a)和圖b)中的圖像具有相同的比例,但圖b)中沒有顯示THG信號。只有在從較長的~160fs脈沖中重新縮放較低的THG信號后,才有可能獲得高于實驗噪聲基底的圖像,如圖c)所示。在這種情況下,需要高2.5倍的平均激光功率來實現與從較短的50 fs以下脈沖獲得的THG信號的信噪比相當的信噪比來實現。總之,小于50fs脈沖提供了相當高的脈沖峰值功率,這導致了在低得多的平均功率下的最佳信噪比圖像,這反過來減少了光漂白,并延長了細胞活力。

50μm2的校準網格(ibidi) 的三次諧波。
a)47mW,全譜短脈沖 (<50fs;VALO系列)
b)6mW 光光譜限制在10nm帶寬 (~160fs)
c)6mw的激光光譜限制在10nm帶寬(~160fs)
展望
多光子顯微鏡在各種應用中具有巨大的潛力,包括開發未來的診斷篩查系統。VALO系列飛秒激光器在50 fs以下范圍內提供脈沖,并提供前所未有的多光子轉換效率和強大的峰值功率。這反過來又有助于推動無標簽多光子應用的前沿,特別是在三次諧波成像中,因為它能夠實現高靈敏度的擴展活細胞成像和延時測量。
參考文獻
[1] Shuo Tang, Tatiana Krasieva, Zhongping Chen, Gabriel Tempea, Bruce Tromberg (2006), Effect of pulse duration on two-photon excited fluorescence and second harmonic generation in nonlinear optical
microscopy, Journal of Biomedical Optics, 11(2).
[2] Mira Sibai, Hussein Mehidine, Fanny Poulon, Ali Ibrahim, M. Juchaux, J. Pallud, A. Kudlinski, Darine Haidar (2018), The Impact of Compressed Femtosecond Laser Pulse Durations on Neuronal Tissue Used for Two-
Photon Excitation Through an Endoscope, Scientific Reports, 8:11124.
[3] G.M Hale and M. R. Querry (1973), Optical Constants of Water in the 200-nm to 200-microm Wavelength Region, Appl. Opt., 12, 555-563.
[4] Gert-Jan Bakker, Sarah Weischer , Júlia Ferrer Ortas, Judith Heidelin, Volker Andresen, Marcus Beutler, Peter Friedl (2022), Intravital Deep-Tumor Single-Beam 2-, 3- and 4-Photon Microscopy, eLife 11.
[5] K. Giering , O. Minet , I. Lamprecht , G. Müller (1995), Review of thermal properties of biological tissues, SPIE PM, 25, 45-65.
[6] Stephen A. Boppart, Sixian You, Lianhuang Li, Jianxin Chen, and Haohua Tu (2019), Simultaneous label-free utofluorescence-multiharmonic microscopy and beyond, cAPL Photon 4.

